

世界の臨床研究の
歴史から最新動向から

糖尿病再生医療とは、細胞・組織の再生や移植を通じ、既存の薬物療法やインスリン注射などの対症療法では解決できない「欠損の補填」や「組織再建」を目指す領域です。
その主なターゲットは、β細胞が破壊され消失した1型糖尿病患者や重度長期の2型糖尿病患者で、インスリン分泌可能なβ細胞の再生に成功すれば、根治、あるいは大幅なインスリン依存度の大幅な軽減が期待できます。
この大命題に対し、米国を中心に30年以上前から、ドナーからの膵島移植や多能性幹細胞(ES細胞・iPS細胞)から分化誘導させた膵島β細胞の移植、さらに最大の懸案である免疫制御策など多様なアプローチの臨床研究が試みられてきました。
本ページでは、糖尿病再生医療に関する世界の臨床研究の歴史や最新動向について糖尿病専門医が詳しく解説した上で、当院が提供している間葉系幹細胞治療の作用の本質や期待される効果と限界などについて端的に説明します。

幹細胞再生治療を通じ、国民病で万病の元である糖尿病の根治に取り組んでいる。
■職歴:
西暦2012年1月〜:東京女子医科大学病院 初期研修医
西暦2015年4月〜:医療法人貞心会
西山堂慶和病院勤務
西暦2019年4月〜:海老名総合病院糖尿病センター勤務
西暦2020年4月~:東京女子医科大学病院糖尿病・代謝内科助教
西暦2022年1月〜現在:一般社団法人輝実会
青山レナセルクリニック院長
■所属学会等
日本内科学会
日本糖尿病学会
日本再生医療学会
糖尿病眼学会
日本内科学会認定内科医(認定番号107827)
日本糖尿病学会専門医(認定番号7237)
最新の推計では、現在、世界中の成人(20–79歳)のうち、約5億8900万人が糖尿病を患っていると報告されています。このうちの90%以上が2型糖尿病ですが、この背景には、肥満・高齢化・都市化などがあります。
いっぽう、自己免疫作用により膵臓のインスリンを産生するβ細胞が破壊されている1型糖尿病も急増しており2040年までに1,700万人まで倍増すると予測されています。
日本においても、ボーダーと呼ばれる糖尿病予備軍も含めると約2,300万人と推定され、成人の5人に1人が該当します。
糖尿病は、放置しておくと、網膜症、腎症、神経障害などの微小血管疾患をはじめとする慢性合併症を引き起こします。また、長期間にわたる高血糖に起因する動脈硬化により心筋梗塞や脳梗塞などの死亡リスクが高まります。
日本糖尿病学会が10年単位で集計している大規模調査によれば、糖尿病患者の平均寿命は、非糖尿病患者と比べて、男性で-7.2才、女性で-10.4才と顕著に短くなっています。
(日本糖尿病学会 大規模調査 2022〜2020年データ)
男性
女性

現在、世界中の成人(20–79歳)のうち約5億8900万人が糖尿病を患っており、日本国内でも予備軍を含めると成人の5人に1人にあたる約2,300万人と推定されています。
糖尿病は放置すると網膜症、腎症、神経障害などの「三大合併症」を引き起こすだけでなく、動脈硬化を進行させ、心筋梗塞や脳梗塞などの致命的な疾患リスクを有意に高めます。この慢性的な高血糖状態が、統計的な寿命短縮の主な要因と考えられています。
このように、世界人口の高齢化に伴い、特に2型糖尿病患者が顕著に増加すると予想されており、既存の治療法に代わるより良い治療オプションに対するニーズが高まっています。
本ページでは、新しい糖尿病治療の選択肢として期待されている「糖尿病再生医療」に関する臨床研究の歴史や最新動向から当院が提供する間葉系幹細胞(MSC)を用いた治療のエビデンスまで専門医が詳しく解説します。
糖尿病は複数のタイプとさらに細かなサブタイプに分類されます。本ページは糖尿病再生医療の目標や世界の研究動向、治療効果の検証などをテーマとしていますが、前提となる糖尿病の種別についての正確な理解が必要なため、簡単に説明します(既にご存じの方は読み飛ばして下さい)。
糖尿病は、「1型」「2型」の主分類に加えて、「その他の糖尿病」として「若年発症の遺伝性糖尿病(MODY)」「妊娠糖尿病(GDM)」「二次性糖尿病(薬剤性など)」に大別されます。
ここでは、1型と2型を対象に解説します。
膵臓の95%以上は消化酵素を分泌する腺房組織で構成されていますが、その中に、ランゲルハンス島(または「膵島」)と呼ばれる無数の組織が島のように点在しています。
膵島は、役割の異なるα細胞、β細胞、δ細胞と豊富な毛細血管で構成されていますが、このうちインスリンを分泌するβ細胞が、自己免疫によって破壊され、ほぼ消失してしまうのが1型の病態です。


治療法は、自己注射による継続的なインスリン補充で、持続皮下インスリン注入(CSII:インスリンポンプ)やインスリン頻回注射療法(MDI)、連続血糖モニタリング(CGM)や自動インスリン注入システム(ハイブリッドクローズドループ)の併用により血糖を最適化します。

加えて、血糖自己管理教育、栄養と運動指導、低血糖対策、合併症(網膜症・腎症・神経障害・心血管疾患など)の定期スクリーニングと管理が重要です。
研究面では免疫療法(自己免疫の抑制・寛容誘導)、膵島・膵移植、幹細胞由来β細胞移植、免疫回避技術や再生医療の開発が進められています。
1型糖尿病は、さらに以下の3種類に分類されますが、いずれも「自己免疫異常」である点が共通です。「緩徐進行型」のように、一見、2型と見分けがつかない場合でも、血液検査で容易に判断できます。すなわち、自己抗体指標である抗GAD抗体、IA-2抗体、ZnT8 抗体が陽性なら、数値に関係なく1型です。


| サブタイプ | 概要 | 症状・特徴 | 発病年齢 |
|---|---|---|---|
| 急性発症1型 |
|
|
|
| 緩徐進行1型 |
|
|
|
| 劇症1型 |
|
|
|
※横にスクロールできます
全糖尿病患者の90%以上を占める2型糖尿病は、俗に「生活習慣病」と呼ばれるように、肥満や高脂質が原因で、膵臓から分泌されたインスリンに対する感受性が低下(インスリン抵抗性が上昇)することで血糖をコントロールできなくなる代謝異常ですが、進行するとインスリン分泌も低下します。
インスリン抵抗性


また、肥満以外でも遺伝的素因、運動不足、ストレス、睡眠障害、一部の薬剤(ステロイドなど)、及び脂肪分布の異常(内臓脂肪増加)などが発症に関与します。
初期は自覚症状が乏しく、放置すると多血糖による多飲・多尿・体重減少や疲労感のほか、長期的には心血管疾患、網膜症、腎症、神経障害、足病変などの合併症を招きます。
治療は、生活習慣の改善と、個々の患者の病態や合併症リスクに応じて各種経口血糖降下薬及び注射薬を組み合わせて段階的に行います。経口薬や注射薬で十分な血糖コントロールが得られない場合はインスリン療法を採り入れます。治療目標(HbA1c値)は年齢、合併症、低血糖リスク、生活状況に応じて個別化されます。早期発見・早期介入と継続的な管理により合併症リスクを低減し、生活の質を維持することが重要です。
同じ2型糖尿病でもインスリン分泌不全が主因の群とインスリン抵抗性が主因の群では有効な薬剤や生活指導が異なるため、病型に応じた精密な治療選択が必要となります。加えて、各サブタイプは網膜症・腎症・心血管疾患など合併症リスクや進行速度が異なるため、スクリーニング頻度や介入の強度を調整して予後を改善できます。
| サブタイプ | インスリン分泌 | インスリン抵抗性 | 特徴 |
|---|---|---|---|
| 「SIDD」 重度インスリン分泌不全型 |
著しく低下 | 軽度~中等度 |
|
| 「SIRD」 重度インスリン抵抗性型 |
高め | 顕著に上昇 |
|
| 「MOD」 軽度肥満関連型 |
軽度低下~正常 | 軽度~中等度上昇 |
|
| 「MARD」 軽度高齢発症型 |
軽度低下 | 軽度上昇又はほぼ正常 |
|
※横にスクロールできます

縦軸:HOMA2-B インスリン分泌(高いほど健全)
横軸:HOMA2-S インスリン感受性(高いほど健全)
糖尿病患者に対する一般的な治療法である生活習慣病の管理及び経口薬、注射薬、インスリンなどは、血糖コントロールと合併症の抑制にある程度有効ですが、限界もあります。
まず、β細胞機能そのものの回復を通じた進行の阻止や根治の手段はなく、根本的治療ではないこと、長期的な薬剤依存に伴う低血糖や体重増加等の副作用や薬剤効果の低減などの問題もあります。
また、適切な治療を行っていても、合併症進行を防げない患者が存在し、生涯にわたって医療負担が継続するケースも少なくありません。
これが「糖尿病は一度罹患したら治らない」「生涯付き合う病気」と言われる所以であり、既存の治療法は全て対症療法と言えます。
これに対し、再生医療は「根治」あるいは「薬剤依存度の大幅な軽減」を目指す治療で、薬剤が届かない「欠損の補填」や「組織再建」を担うものです。
具体的には、失われたβ細胞や機能低下したβ細胞を補充・再生し、内因性インスリン分泌を回復・改善することで、病態の部分的あるいは完全な機能回復を目指します。
ただし、現時点では治験及び研究段階の手法が中心で、既存薬療法や生活習慣療法との併用や補完的に使われており、標準治療を置き換える段階には至っていません。
糖尿病再生医療が標的としている典型的なターゲットは、「1型糖尿病患者」と「長期で重度の2型糖尿病患者」です。
ターゲット01
自己免疫で膵β細胞が大幅に破壊されているため、β細胞数を再生できれば根治に近い改善が期待できることから、最も明確な再生医療の適応候補です。
ドナー膵島移植はドナー不足と免疫抑制の副作用で広範適用が困難であるため、代替・補助的治療に対する強いニーズがあります。
ターゲット02
β細胞機能が著しく低下している患者や膵切除後の糖尿病(外科的欠損)など。
β細胞機能低下と微小血管障害が問題ですが、既存の治療法では組織の修復や保護に対応できないため、根本的な解決手段が求められています。
なお、今後は、長期かつ重度の患者だけでなく、予防目的や機能低下初期の回復を狙うケースにも拡大適用される方向です。
今後は、長期かつ重度の患者様だけでなく、予防目的や機能低下初期の回復を
狙うケースへの拡大適用も期待されています。
最重要課題はβ細胞の再生ですが、以下のとおり多様な方向から研究や臨床が進められています。
β細胞の再生
内因性の再生誘導、細胞移植、幹細胞由来β様細胞の作製・移植
免疫制御
自己免疫反応の抑制・寛容誘導
1型では自己免疫が再発すると移植や再生が持続しないため、免疫調整が必須。
細胞保護・微小環境改善
膵島血管・微小循環系、抗炎症や抗線維化など
α細胞やδ細胞の機能改変
α→β転換など細胞運命変換の研究
バイオエンジニアリング
カプセル化デバイスによる免疫遮断等
遺伝子治療
インスリン産生遺伝子を他組織に導入する等
以下では、特に、幹細胞を使用したアプローチとして「β細胞の再生」と「細胞保護・微小環境改善」を中心に詳しく解説します。
糖尿病に対する再生医療の研究は、1970年代の膵臓・膵島移植の臨床研究に端を発します。
その主要なテーマが「破壊され消失したβ細胞の再生」であることから、常に免疫制御問題の解決が最重要課題と位置付けられてきました。
膵島・膵移植の臨床化と課題の把握(免疫抑制の必要性、ドナー不足)
「Edmontonプロトコル」による膵島移植で一時的なインスリン離脱例が注目されるが、長期維持やドナー供給が課題
恒常的なドナー不足解決のため細胞源多様化の研究が進展
胚性幹細胞(ES細胞)や人工多能性幹細胞(iPS細胞)から膵β様細胞に分化させる技術、細胞カプセル化(免疫隔離)技術、β細胞の増殖・再生促進剤の探索が活発化
臨床移行が進むフェーズに移行
幹細胞由来の移植製品やカプセルデバイス、ブタ(猪)由来異種移植、遺伝子改変(CRISPR)技術・細胞改変による免疫回避、β細胞を誘導する薬剤の臨床開発が並行
このように、糖尿病再生医療に対する臨床研究は、前世紀から継続しており、未だ道半ばですが、その中核となる研究テーマは「ドナーの膵島移植技安定的な術の改良」と「多能性幹細胞(ES細胞・iPS細胞)から作製されたβ細胞の安定的な移植法の確立」です。 以下に、それぞれの研究の経過と最新動向、課題について解説します。
膵臓全体の移植手術の侵襲性を低下させるため、死亡者ドナーの膵臓を酵素処理して膵島を分離し、適合性が認められる患者に移植する治療法。
2000年頃から臨床が本格化し、以後、様々な改良を経て、現在は、肝臓の門脈に対しカテーテルで膵島懸濁液を注入する手技が主流です。


ただし、移植された膵島β細胞の定着率は30~40%程度で、5年後のインスリン離脱率は10~30%程度と報告されています。β細胞単独移植より、α細胞、δ細胞を含む膵島移植の方が血糖が安定しやすいとされています。
【目的】
同種(ヒト)ドナーの膵島移植によるβ細胞の内因性インスリン分泌の復活
【研究及び臨床の経過】
1990s - 2000
1990年代から基礎研究が進められ、2000年にステロイドを最小化した免疫抑制法を用いた臨床移植「Edmontonプロトコル」で、短期的にインスリン離脱を達成する症例が多数報告され、大きなインパクトを与えました。
以降、移植手技や膵島精製・品質管理の標準化、移植直後の炎症反応対策、移植サイトや血管新生促進法の最適化、免疫抑制薬の低毒性化やステロイド回避レジメンの導入など様々な点で改良が進みました。
また、企業主導での大量製造プロセスや細胞保存・供給体制の整備、幹細胞由来β細胞やカプセル化デバイスとの併用を目指す製品開発、臨床試験の実施・規制承認申請も加速しています。
Lantidra
(一般名:donislecel jujn)
2023年6月28日、FDAは「Lantidra」を、「成人の1型糖尿病で反復する重度低血糖(重症低血糖)を改善できず目標HbA1cに到達できない患者」を適応とする医薬品(生物製剤)として承認しました。
これは、ドナー(死亡提供者)由来の同種(ヒト)膵島細胞を用いた細胞療法で、肝門脈へ注入する細胞懸濁液として投与されます。
日本でも大きく報道(報道記事はこちら)
https://www.fda.gov/news-events/press-announcements/fda-approves-first-cellular-therapy-treat-patients-type-1-diabetes https://dm-rg.net/news/1331fef8-df30-417d-862a-5774546fa786?utm_source=chatgpt.com
【課題】
このとおり、ドナーからの膵・膵島移植治療法は、長年にわたって改良が繰り返され、直近ではFDAから医薬品として承認されましたが、以下の課題が残っています。
ドナー不足
適合ドナー供給が限られ、膵島では複数ドナーが必要になる場合もある。
免疫抑制
同種拒絶及び1型糖尿病の自己免疫再発を抑えるため免疫抑制が必須だが、副作用(感染、腎毒性、悪性腫瘍リスク等)が解決されていない。
移植直後の細胞喪失
IBMIR(血液媒介性炎症)や低酸素により膵島は大量に失活しやすい。
生着・血管新生不足
特に肝門脈内移植での酸素・栄養供給不足や十分な血管化の欠如が機能低下を招く。
長期耐久性
移植後のインスリン非依存性の長期維持が限定的で、機能低下が起こり易い。
品質・標準化
膵島調製・保存・評価のバッチ間変動、GMP準拠の製造管理が必要。
「2010年代研究加速 / 2020年代臨床移行〜現在」
2000年代後半になると、恒常的なドナー不足問題を解決する方法として、*多能性幹細胞から人工的にβ細胞を分化させる臨床研究が本格化しました。
*生体内のあらゆる組織の細胞に分化できる万能の細胞のこと。もとは受精卵の内部分裂開始から約5日目に形成される内部細胞塊の中の胚性幹細胞のことで、最終的に胎児のあらゆる臓器や組織の細胞に分裂していきます。
このうち、ES細胞由来の治療法は、ドナーの受精卵から、あらゆる細胞に分化可能な胚性幹細胞を分離してインスリン分泌可能なβ様細胞に分化誘導するものです。

いっぽう、iPS細胞由来の治療法は患者本人の生体内から採取した細胞に遺伝子操作を加えて胚のような多能性細胞に再プログラミングした上でβ様細胞に分化誘導する手法です。
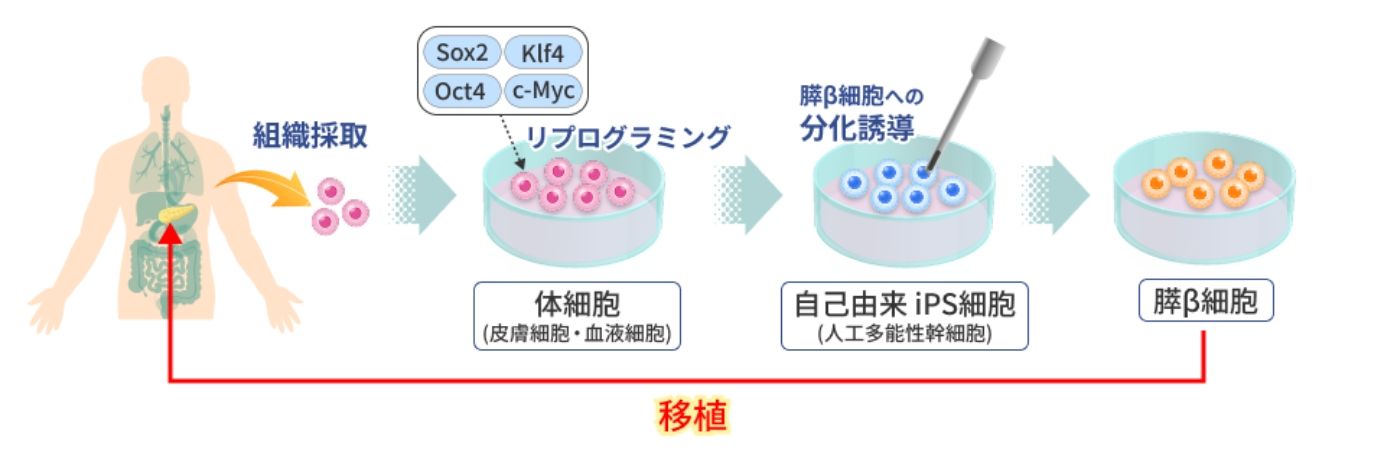
【目的】
大量生産が可能な多能性幹細胞を活用し、長年の課題であった「膵島移植ドナー不足問題」の根本的な克服
【研究及び臨床の経過】
2008年頃から本格的に基礎研究が開始され、2014年以降、ヒト多能性幹細胞(ES細やiPS細胞)からインスリン分泌β様細胞への分化誘導的プロトコルが確立したことで、再生医療向けの大量供給が現実化しました。
その後、米国のベンチャー企業主導で、成熟β細胞製剤(例:Vertex社の「VX 880」)や免疫遮断のためのカプセル化デバイス(例;ViaCyte社の「PEC-Encap」「PEC-Direct」)を使用した製品の臨床展開が進められています。
単なる細胞供給に留まらず、カプセル化デバイス等のバイオエンジニアリング技術を組み合わせることで、
免疫抑制剤に頼らない安全かつ持続的な治療の実現が近づいています。
Vertex Pharmaceuticals社が開発する同種ヒト胚性幹細胞(ES細胞)由来の分化済みインスリン産生膵島様細胞を移植する治療法で、肝門脈注入により投与し、移植細胞の持続には免疫抑制が必要とされる。
【臨床開発状況】
2024年11月、第III相試験開始を発表(主要試験は約50例規模として設計された無作為化/対照設定の大型試験に移行する意向を表明)
これに先立つ第I/II相では、症例数が少なく追跡期間も限られるものの、移植後に血中C ペプチド上昇、インスリン必要量の低下、一部症例で一定期間のインスリン離脱を得た例が報告されたため、第III相へ移行。 最終的には第III相試験を経て医薬品として承認・実用化を目指す段階に移行している。 同種ES由来製品のため大量製造の可能性があり、供給面での利点が期待される。
【主な課題・リスク】
免疫抑制
同種移植のため長期免疫抑制(あるいは免疫回避技術の開発)が前提で、副作用(感染、腫瘍化リスク増加等)の管理が必要
投与法のリスク
肝門脈注入に伴う手技的リスク(門脈塞栓など)。
長期持続性と耐久性
移植細胞の長期生着・機能持続と安全性(腫瘍化リスク含む)はまだ不確定で、長期フォローが必要である
副作用を伴う免疫抑制剤なしにβ細胞を移植するため、細胞をバイオカプセル化して免疫から遮蔽する技術や局所免疫調整デバイスの開発が進んでいます。
その中核であるViaCyte社(後にVertex Pharmaceuticals社が買収)は、ES細胞由来の膵島前駆体をカプセルに封入した皮下埋入型デバイス(皮下や腹腔内に移植)を開発しました。



2016年以降、初期臨床試験が本格化。ViaCyte社は、「PEC Encap」(免疫隔離型)で第I/II相試験を進めたところ、デバイスの安全性は示されたが十分な分化・機能化(血中C ペプチド検出)や血管化の欠如、周囲の線維化による機能低下が課題であると報告されました。

一方の「PEC Direct」(免疫抑制併用型)では、移植後のC-ペプチド上昇の報告があり、免疫隔離と機能維持のトレードオフが露呈したことになります。
並行してアルギン酸の化学修飾(高純度アルギン酸、免疫反応低減化)、コンフォーマルコーティング技術、透過性を最適化した半透膜、表面抗炎症処理、局所免疫調節薬埋め込み(サイトカイン中和、CXCL12発現など)やTreg誘導併用の研究が進展。
臨床的には複数の企業・学術グループが皮下埋入型デバイスの早期試験を実施中ですが、十分なインスリン分泌機能と長期持続性を同時に達成するエビデンスはまだ確立していません。
移植したデバイス周辺の組織の線維化や血管新生の不足による酸素・栄養供給不足のため、
移植したβ細胞の機能低下を引き起こす事例が多く、今後の課題となっている。
いずれも、あらゆる細胞に分化できる「多能性幹細胞」ですが、糖尿病再生医療としての現時点の臨床進行度は「ES細胞由来のβ細胞」が相対的に先行しています。
理由は、ES細胞は臨床グレードの確立した細胞株を使用した大量製造・品質管理体制整備しやすい点、長期にわたる均一な分化プロトコルの確立による製造の安定性など主に供給面の利点にあります。
また、初期臨床で先行するVertex社などの米系企業がES系プラットフォームを採用しており、臨床試験開始が早かったという事情もあります。
いっぽう、iPS細胞は、患者自身の細胞を利用するため免疫適合や胚を使用する倫理的問題が無い点で優位ですが、個体差に依存するため大量製造、分化の均質化・安定化が困難なこと、腫瘍化リスク管理などでESより開発開始が遅れる傾向があります。
ただし日本ではiPSC臨床研究・治験の動きが活発で、iPSC由来β細胞の臨床化を目指す取り組みが進行中です。
長期安全性、免疫対策や倫理面などを踏まえ、将来的にはiPSCアプローチも重要な役割を果たす可能性が高いと言えます。
| ES細胞由来 | iPS細胞由来 | |
|---|---|---|
| 製造方法 | 同種(ヒト)ドナーの受精卵から胚性幹細胞を抽出しβ細胞に分化誘導 | 患者自身の体内から採取した細胞を再プログラミングして胚性細胞を作製しβ細胞に分化誘導 |
| 利点 |
|
|
| 問題 |
|
|
糖尿病再生医療の近未来のゴールは、安全で効果的なβ細胞補充療法を確立することです。具体的には、移植や細胞療法により持続的にC‑ペプチドを回復させ、インスリン需要を大幅に低減、あるいはインスリン離脱を達成することを目指します。
また、糖尿病再生医療の最重要課題である、全身免疫抑制に依存しない治療法の実現が不可欠で、免疫を制御しうる細胞、局所免疫調節デバイス、完全な免疫隔離技術などによって免疫抑制の最小化または不要化を図ることが最終的なゴールと言えます。
これを実現するための条件として、まず供給面でES/iPS細胞由来β細胞の安定した大量生産と品質保証(未分化細胞の除去や均一な機能性・安全性の担保)を確立する必要があります。
安全面では腫瘍化や感染などの長期リスクを評価・管理し、移植細胞の長期生着と機能耐久性を示すエビデンスを蓄積することが求められます。

現実的な目標としては、短期的には、多能性幹細胞由来β細胞製剤の数年内の第III相試験による有効性・安全性の確立と限定的承認。5–10年の中期では免疫抑制軽減技術やデバイスの臨床実装と供給体制整備、10年以上の長期では広範囲な臨床適用と保険償還を伴う実用化が見込まれます。
前記のとおり、現在、膵島β細胞の再生を目指す様々なアプローチが試行されていますが、長期安定性や免疫対策を
はじめ課題が山積しており、実現にはまだ相当な時間を要するのが実情です。そこで、これらの臨床研究と並行して、免疫に対する抵抗性が高く、腫瘍化リスクをはじめとする安全面の懸念が少ない手法として注目されたのが患者自身の間葉系幹細胞を使用した糖尿病再生医療です。
現在、当該治療は、日本をはじめ複数の国で自由診療として広く提供されており、それらの臨床評価が進んでいます。
生体内の骨髄、脂肪、臍帯、歯髄などに存在し、同じ性質の細胞に分裂できる「自己複製能」と、軟骨・骨・脂肪などの一部の組織細胞に分化することができる「多分化能」の特殊な能力を併せ持つ細胞のことです。

胚性幹細胞に代表される多能性幹細胞と比較すると、分化能には限界があり、内胚葉系の細胞である膵島β細胞への分化は期待できません。
いっぽう、間葉系幹細胞は、「パラクライン効果」と「免疫抑制効果」という極めて優れた作用機序を有しており、この点に着眼して、近年、再生医療に広く利用されています。
間葉系幹細胞(MSC)は、糖尿病に対して主に以下の効果が期待できます。
MSCは、直接免疫細胞に作用し、あるいは成長因子の分泌を通じて免疫調整を行うため、特に1型における自己免疫抑制の補助効果が期待できます。
MSCには、数百種類の成長因子やサイトカイン、エクソソームなどの生理活性物質を分泌して長期間の高血糖で傷ついた組織の修復や炎症抑制、血管新生を促進するパラクライン効果と呼ばれる優れた作用があります。


この結果、特に2型糖尿病の背景にある代謝環境の改善を通じたインスリン抵抗性の低減や、難治性潰瘍、足壊疽、腎症などの糖尿病性合併症の改善にも有用との報告が多数あります。
MSCが分泌する数百種類の生理活性物質の中で、特に糖尿病に対して有用な成長因子・サイトカインとして以下が挙げられます。
VEGF
(血管内皮細胞増殖因子)
損傷した血管内皮細胞の修復や新生を促進することによる血流、微小循環の改善
HGF
(肝細胞増殖因子)
血管保護、抗線維化作用による組織修復
IGF-1
(インスリン様成長因子)
損傷した血管内皮細胞の修復や血管新生の促進による血流改善、潰瘍治癒促進
TGF-β
(トランスフォ―ミング成長因子)
創傷治癒と線維化制御による炎症抑制
IL-10、ID0等
(免疫抑制性サイトカイン)
炎症抑制・免疫寛容化の促進
MSCを用いた糖尿病治療は、2000年代後半〜2010年代にかけて本格化し、最初は小規模臨床試験や安全性試験が中心でした。MSCは、体内の骨髄、脂肪、歯髄、臍帯組織などから比較的容易に採取可能で、大量製造しやすい点、免疫抵抗性が高く、自家移植のため安全性が高いことから臨床応用が加速しました。投与法は静脈注射(点滴)が主流ですが、足の潰瘍に対する局所注入など用途に応じた投与経路が試みられています。
また、短期的な重大有害事象が少なく安全面は良好と報告される一方、長期の腫瘍化リスクや細胞の均質性・品質管理は検証継続中です。
参考①:https://pubmed.ncbi.nlm.nih.gov/32926576/
参考②:https://europepmc.org/article/med/40462158
間葉系幹細胞を使用した糖尿病再生医療が本格的に開始された2000年代後半~2010年頃は、小規模臨床試験や安全性試験が中心でしたが、その後、多数の臨床報告やそれらを統合した解析が発表され、糖尿病や合併症に対する効果についての評価が進んでいます。
小規模非ランダム化試験で1型糖尿病患者のHbA1cやインスリン必要量の一時的低下、C-ペプチドの若干の改善が報告されました。
【要旨】
1型糖尿病患者に対して、臍帯由来間葉系幹細胞と自家骨髄単核細胞の膵動脈内への投与と標準治療の併用療法の有効性と安全性を評価したランダム化比較試験
【結果】
1年間の追跡調査において、移植群では各糖代謝指標において極めて有意な改善が認められました。
c-ペプチドAUC
約2倍(+105.7%)に増加
β細胞機能が改善し、インスリン分泌が改善
インスリン分泌能
+49.3%改善
HbA1c
8.6% → 7.5%
(−1.1%、約12.6%相対低下)
インスリン必要量
約29%減少
空腹時血糖
約24%低下
一方、標準治療のみの対照群では:
以上のとおり、両群間には明確な差が確認されました。
【安全性】
重篤な有害事象は少なく、手技および細胞投与は概ね忍容可能と報告されている。
【評価】
本治療による効果は、幹細胞が直接β細胞へ分化したのではなく、免疫調整作用や膵島微小環境の改善、炎症抑制による残存β細胞機能の保護・回復が関与した可能性が示唆されています。
2010年代半ばになると、重症の糖尿病性足潰瘍や虚血性病変に対するMSCの局所投与で潰瘍治癒率の改善や切断回避効果を示す報告が相次ぎ、MSCの局所投与の有望性が示されました。
【要旨】
糖尿病足潰瘍に対する間葉系幹細胞(MSC)療法の有効性に関する複数のランダム化比較試験の*メタ解析
*複数の信頼度の高い臨床試験を統合し、MSC治療の効果を総合評価した論文のこと

【結果】
創傷の完全治癒率の改善について
全体の改善度
(95% CI: 1.23~2.16)
MSC治療を受けた場合、完全癒合の可能性が1.63倍に高まることを示唆。
MSC療法は通常治療に比べて創傷の完全治癒率を有意に高めることが示された。
小さな潰瘍
小さな潰瘍(5cm²未満)に対する効果
(95% CI: 1.11~2.63)
通常治療に比べて、MSC治療による癒合効果がさらに高く現れた。
大きな潰瘍
大きな潰瘍(5cm²以上)に対する効果
(95% CI: 0.75~1.86)
統計的な有意差は見られず、明確な改善効果は示されなかった。
長期的な重大合併症について
現時点ではMSC療法が明確に有利とは判断できない。
【評価】
このメタ解析では、MSC療法が、創傷(足の潰瘍)が治る確率を高める可能性があり、特に比較的小さな潰瘍ほど効果が出やすい傾向が示唆されました
多数の小規模試験を統合したメタ解析で、安全性は支持される一方で血糖コントロール改善(HbA1c・インスリン使用量)の効果は一貫性に欠け、効果サイズは小〜中等度であること、被験者や投与法によるばらつきが大きいと結論づけられています。
【要旨】
1型及び2型糖尿病患者に対して間葉系幹細胞(MSC)療法の血糖管理やインスリン分泌、薬の必要量などの指標に対する効果を評価した無作為化比較試験を統合したメタ解析。信頼性の高い13件の臨床試験における合計507人の糖尿病患者(うち1型:199人、2型:308人)が解析対象。
各研究で、MSC療法を受けた群と通常治療・プラセボ群での効果を比較した。
HbA1c
MSC療法群
平均 -0.72%
インスリン必要量
MSC群では1日あたりインスリン使用量
-14.5単位減少
C-ペプチド
MSC群でC-ペプチド値が平均
+0.24ng/mL上昇
食後血糖
MSC群で平均
平均 -11.32mg/dL
空腹時血糖
両群に有意差なし
【評価】
間葉系幹細胞(MSC)療法は、1型・2型糖尿病患者の血糖管理を改善し、HbA1cを平均約0.7%低下させ、インスリン使用量や内因性インスリン分泌の改善にも寄与する可能性が示されました。ただし、空腹時血糖への影響は明確ではなく、さらなる大規模・長期試験が必要です。
糖尿病が進行すると、腎臓の機能が低下し尿タンパクや腎機能障害が出る「糖尿病性腎症」をきたすことがあります。既存の治療だけでは十分な改善が得られないケースもあり、新しい治療法として間葉系幹細胞(MSC)療法が注目されています。
MSC投与による腎保護効果のシグナルを示す報告が多数あり、MSCの分泌物(成長因子やエクソソーム等)による作用機序も示唆されています。
【要旨】
糖尿病性腎症に対するMSC療法の効果に関する系統的レビュー/メタ解析


【結果】
腎機能の改善や腎障害の緩和が示された。
血清クレアチニン(SCr)
低下
尿素窒素(BUN)
低下
尿中タンパク量
低下
腎線維化の抑制
・MSC療法の腎線維化を軽減する効果が示唆された
【評価】
MSC治療が、尿蛋白や血清クレアチニン、尿素窒素の改善と線維化抑制を通じて血糖値や腎機能指標を改善する報告が多数あり、MSC治療は糖尿病性腎症に対する将来有望な治療法の候補であることが示されました。
また、MSCの分泌物(成長因子やエクソソーム等)による機序(パラクライン効果)も示唆されています。
過去の臨床報告においては、間葉系幹細胞の膵島β細胞への分化は否定されており、MSCから分泌される生理活性物質(成長因子、サイトカイン、エクソソーム)によるパラクライン効果が示唆されています。
多数の研究はMSCが長期的に膵β細胞に直接分化して機能的インスリン産生細胞になるという証拠は乏しいとし、MSCの主要作用は別機序であると示唆しています。
参考(2014年):https://link.springer.com/article/10.1186/s12967-014-0260-8
MSCは抗炎症性サイトカイン、成長因子、免疫調節分子を分泌し、局所の炎症軽減、血管新生促進、線維化抑制、β細胞の保護・機能回復を媒介することが多くの臨床データで支持されています。
この論文は、パラクライン効果による膵臓の保護作用を示したものです。骨髄由来間葉系幹細胞移植は、糖尿病モデルにおいて血糖改善効果を示しましたが、その作用機序としてβ細胞への直接分化ではなく、分泌因子による傍分泌作用が中心である可能性を検証した実験研究です。MSCの血糖改善の作用機序はβ細胞への直接分化ではなく、分泌因子による傍分泌作用が中心である可能性、パラクライン効果による膵臓の保護作用が示されました。
MSCはT細胞やマクロファージの機能を修飾し、自己免疫反応や移植後の炎症を緩和する可能性を持つが、持続的免疫寛容を単独で作るエビデンスは限定的としています。
MSC単独での長期的インスリン非依存化を示す明確なエビデンスは存在しません。
短期的なC-ペプチド上昇やインスリン量の軽減を示す報告はあるものの、再現性は限定的。今後は、免疫調節作用を目的とした併用試験が注目されています。
インスリン抵抗性や慢性炎症を背景とするタイプでHbA1c低下、インスリン感受性改善を報告する小規模試験は多数あるものの、大規模試験での確証は十分とはいえません。
局所MSC投与は潰瘍治癒率向上や血行改善、切断回避に有効な報告が多く、最も臨床応用の期待が高い分野の一つと目されています。
自家間葉系幹細胞を用いた糖尿病再生医療は、安全面で有望で、インスリン抵抗性型の2型糖尿病や合併症(特に腎症などの虚血性病変、足潰瘍など)に対しては十分な効果が期待できます。
一方、MSCのβ細胞への直接分化はほぼ否定されており、血糖コントロール改善を目的としたMSC単独療法は有効性が一貫していないため、主な作用機序であるパラクライン効果や免疫調整の臨床へ最適化が今後の鍵と考えられます。
当院では、これらの科学的知見に基づき、間葉系幹細胞による糖尿病治療を行っています。
多数のエビデンスが示すように、間葉系幹細胞による糖尿病再生医療は、β細胞再生を目的とした治療ではなく、炎症抑制作用と微小循環改善を介してインスリン感受性を高める「代謝環境改善療法」と位置付けています。
その結果、必要インスリン量の減量や離脱、血糖コントロールの改善、さらに残存しているβ細胞の保護(アポトーシスの抑制)が期待できます。
また、作用機序の中心はパラクライン効果ですから、成長因子やサイトカインの補強のため、院内で製造している幹細胞培養上清液(エクソソーム)を併用しています。
パラクライン効果による代謝改善や組織の炎症修復を通じたインスリン抵抗性の改善が期待できます。
免疫調節によるβ細胞温存の可能性が期待できます。

MSCが分泌するHGF等による炎症抑制やVEGFの血管新生効果による微小環境の改善が期待できます。
海綿体局所投与による血流改善や神経保護を通じた組織修復効果が期待できます。
MSCが分泌するVEGFによる血管新生促進が期待できます。